HSC 刷题开始!周一【化学】
- May 12, 2018
- 2 min read
从今天开始,我们会和HSC考试分享Past Paper ,不废话,开始!



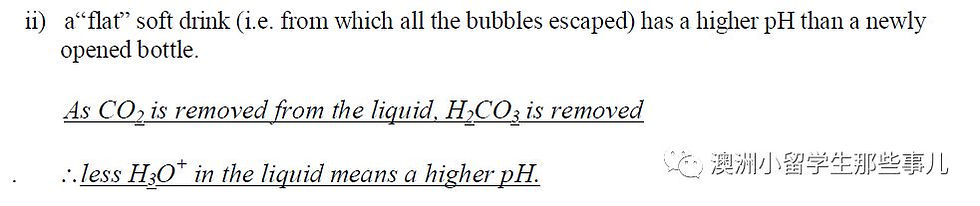
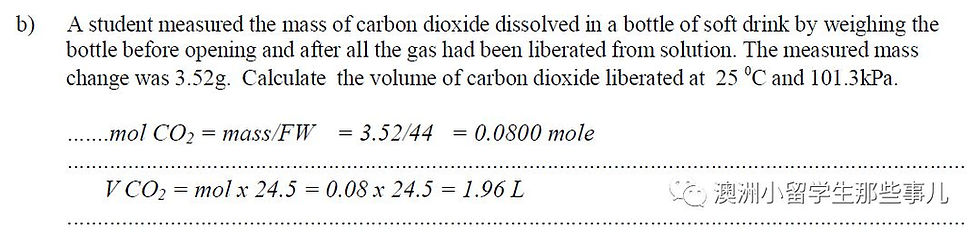

这道题目需要学生对于二氧化碳,水以及碳酸之间的平衡有一定的了解。日常生活中的碳酸饮料就结合了这三样东西。在封闭的状态下,二氧化碳,水以及碳酸处于一个平衡的状态。一旦瓶盖被打开,平衡就会遭到破坏,压力的变化会导致碳酸变回二氧化碳。
A部分的第一部分问到用 Le Chatelier 的定理,解释为什么但碳酸饮料被打开后,会有泡沫产生。
学生们首先要知道什么是Le Chatelier 的定理。 Le Chatelier的定理说明,当一个封闭的系统有了压力,温度,浓度,容量的改变后,相关的平衡也会有所改变。
当瓶盖被打开后,系统的压力会大大减少,平衡度会走向左边,制造更多的水和二氧化碳。当二氧化碳从饮料中出现时,就会有泡沫的现象。
第二部分问道,为何跑气了的饮料的pH值会比刚刚打开的饮料的要高。
学生们只要记得碳酸饮料的气是由饮料里面的碳酸变成的。当气跑走时,碳酸的数量也会下降,pH值就会增高。
B部分需要学生通过饮料重量的变化来到找出已经排放出的二氧化碳量。 学生首先会要找出二氧化碳每摩尓的重量 (12 + 16 + 16=44克)。 3.52克相当于0.08摩尓。我们知道在25摄氏度的情况下,每摩尓的容量相当于24.5 公升的气体。所以流失了的二氧化碳的容量是1.96公升。
C部分问道学生酸雨的形成会产生什么样子的影响。同学们可以自己想一想,把想好的答案发给我们的公众号,会有老师为大家解答。
如果你对于化学有问题或疑问……

快快加微信,加入我们的Tutoring Centre一起补习吧!
咨询电话:0404 602 351































Comments